Commento all’articolo: LATS1-modulated ZBTB20 perturbing cartilage matrix homeostasis contributes to early-stage osteoarthritis. Hao X, Zhao J, Jia L, Ding G, Liang X, Su F, Yang S, Yang Y, Fan J, Zhang WJ, Yang L, Jie Q. Bone Res. 2025 Mar 12;13(1):33. doi: 10.1038/s41413-025-00414-3. PMID: 40069162; PMCID: PMC11897192.
L’osteoartrite (OA) è una patologia cronica a carico delle articolazioni ed è una delle maggiori cause di disabilità al mondo. La patologia si caratterizza per l’insorgenza di cambiamenti patologici che vedono la formazione di fibrillazioni, la degenerazione della cartilagine articolare, la formazione di sclerosi a livello subcondrale e di osteofiti oltreché l’insorgenza di infiammazione (1). Analisi di espressione genica hanno dimostrato il potenziale coinvolgimento di ZBTB20, un fattore di trascrizione appartenente alla famiglia delle Zinc Finger e BTB domain-containing protein, nell’infiammazione durante le prime fasi di progressione dell’OA. Nello sviluppo dello scheletro, in modelli murini, ZBTB20 sembra essere coinvolto nella regolazione del differenziamento dei condrociti ipertrofici attraverso la repressione di Sox9, suggerendo, quindi, un suo possibile coinvolgimento nei condrociti della cartilagine articolare in quadri di OA (2,3).
Lo studio di Hao et al. pubblicato sulla rivista Bone Research, descrive il ruolo di ZBTB20 nella progressione dell’OA oltre che identificarlo come possibile target terapeutico.
Gli autori attraverso l’utilizzo, in vitro, di linee cellulari di condrociti primari in cui tramite IL-1b si è indotto il quadro infiammatorio, e in vivo, con modelli murini in cui è stata indotta l’OA tramite dislocazione del menisco mediale (DMM), hanno dimostrato il coinvolgimento di ZBTB20 nelle fasi iniziali dell’OA. Infatti, ZBTB20 nelle prime fasi di sviluppo della patologia, nei condrociti ipertrofici trasloca dal citoplasma al nucleo e gradualmente tende a diminuire con il progredire della patologia.
L’utilizzo del modello murino Col2a1-CreERT2 con delezione di ZBTB20 tramite iniezione di TAM a 10 mesi, dimostra che la delezione del fattore ritarda la progressione dell’OA e a livello della ECM ripristina l’espressione di Coll II e ACAN, mentre blocca l’espressione degli enzimi di degradazione della matrice MMP13 e ADAMTS5.
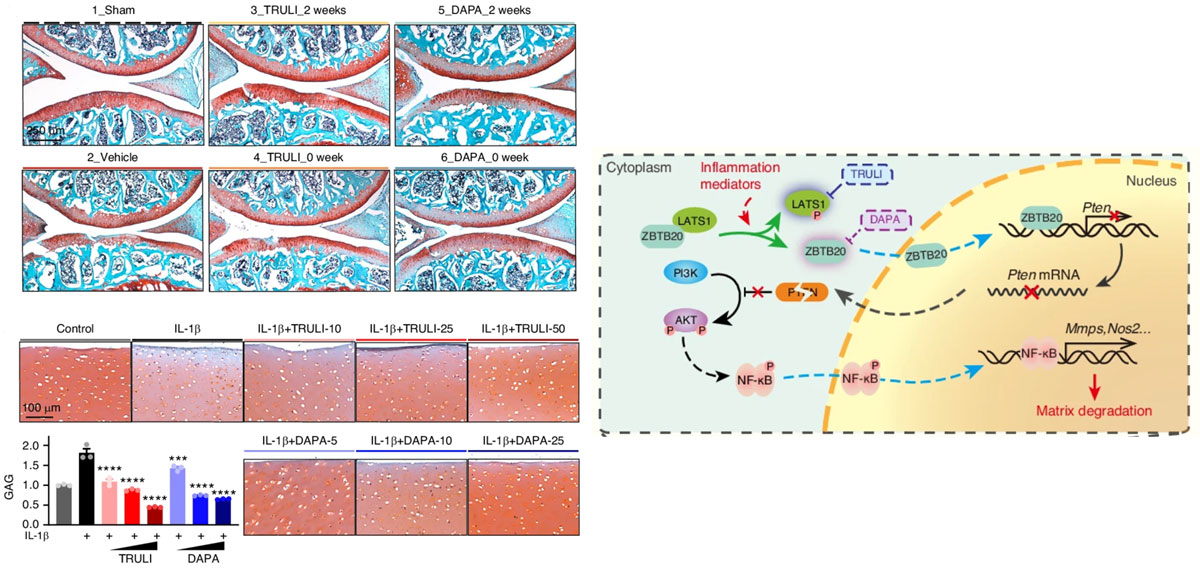
Gli esperimenti in vitro condotti su condrociti articolari, hanno confermato l’effetto negativo del fattore sulla omeostasi della ECM; il fattore, infatti, attiva la via di NF-kB e sopprime Pten con conseguente attivazione della via PI3K-AKT.
In aggiunta, gli studi di espressione genica e trascrittomica hanno dimostrato che a regolare la distribuzione intracellulare di ZBTB20 è LATS1 (Large Tumor Suppressor Kinase 1), uno degli enzimi coinvolti nella regolazione del ciclo cellulare. Analisi in vitro ed in vivo hanno mostrato una elevata fosforilazione di LATS1 che potrebbe causare la redistribuzione di ZBTB20, inoltre gli esperimenti di CO-IP hanno confermato l’esistenza di un’interazione LATS1-ZBTB20. Gli autori hanno mostrato che utilizzando l’inibitore selettivo, TRULI per LATS1/2 si assiste ad un blocco dell’accumulo del fattore a livello nucleare indotto da IL-1b, oltre a mostrare un miglioramento del danno a carico della ECM. Tale dato oltre a confermare il ruolo di LATS1 nella traslocazione nucleare di ZBTB20 identifica nell’inibitore un possibile agente terapeutico per l’OA.
Successivamente gli autori hanno utilizzato il DAPA (dapagliflozin) per valutare i possibili effetti in quadri di OA. In particolare l’utilizzo del DAPA nei condrociti porta ad una riduzione dell’espressione di ZBTB20 e ad un incremento dell’espressione di Pten. Il DAPA, inoltre, permette di mitigare i danni a carico della ECM con un meccanismo dose dipendente suggerendo un suo effetto protettivo nei condrociti osteoartritici.
In conclusione lo studio dimostra che i due indipendenti approcci terapeutici, rispettivamente con TRULI e DAPA, modulando l’espressione di ZBTB20 mitigano i danni degenerativi a carico della matrice cartilaginea e potrebbero in un futuro rappresentare una possibile strategia terapeutica per contrastare gli effetti dell’OA.
- Leifer VP, Katz JN, Losina E. The burden of OA-health services and economics. Osteoarthritis Cartilage. 2022 Jan;30(1):10-16. doi: 10.1016/j.joca.2021.05.007. Epub 2021 May 20. PMID: 34023527; PMCID: PMC8605034.
- Barakat S, Ezen E, Devecioğlu İ, Gezen M, Piepoli S, Erman B. Dimerization choice and alternative functions of ZBTB transcription factors. FEBS J. 2024 Jan;291(2):237-255. doi: 10.1111/febs.16905. Epub 2023 Jul 21. PMID: 37450366.
- Zhou G, Jiang X, Zhang H, Lu Y, Liu A, Ma X, Yang G, Yang R, Shen H, Zheng J, Hu Y, Yang X, Zhang WJ, Xie Z. Zbtb20 regulates the terminal differentiation of hypertrophic chondrocytes via repression of Sox9. Development. 2015 Jan 15;142(2):385-93. doi: 10.1242/dev.108530. PMID: 25564625.